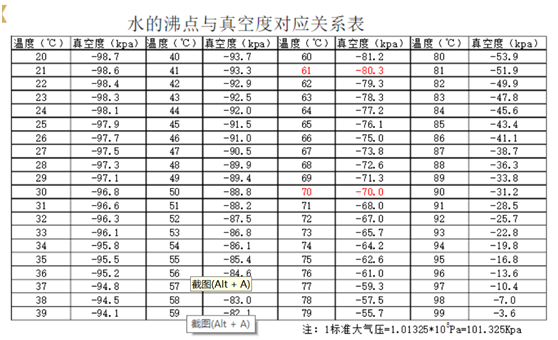
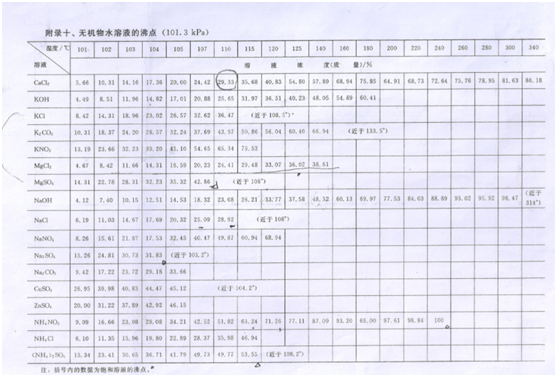
什么是沸點升高?
沸點升高是《物理化學》或者《化工熱力學》中的一個基礎概念,簡單的解釋就是沸點是液體飽和蒸氣壓等于外壓時的溫度。若溶質不揮發,則在同一溫度下溶液的蒸氣壓要小于純溶劑的蒸氣壓。在純溶劑的沸點Tb下,純溶劑的蒸氣壓等于外壓,溶液的蒸氣壓則小于外壓而不能沸騰。要使溶液在同一壓力下沸騰,必須將溫度升高到T>Tb。這種現象即為沸點升高。一般來說,無機鹽濃溶液的沸點升數值較高,稀溶液數值較小。 工業上的蒸發器中涉及到的沸點升高,除去上述的基本概念以外,還有個很現實的問題,由于在蒸發器到加熱器的管道和設備存在液柱,濃溶液比重很大,因此一定的液柱下溶液本身壓力也較高,比重為1的水,10m高就增加1個大氣壓的壓力,此時水的沸點隨著壓力的增加也增加,達到120C了,要是比重為1.5的濃溶液,同樣的液柱將會增加1.5個大氣壓的壓力,此時沸點升就更高,越是濃溶液越是沸點升高數值越大。也就是說在蒸發器實際操作過程中,沸點升高隨濃度即液柱高度而變,濃度越高,業主越高,沸點升數值越高。 至于如何計算,不同的溶質和溶劑有不同的沸點升,一些手冊,比如制鹽工業,海水和鹵水的沸點升高有現成的數據和公式可以查閱和計算,其他的水溶液也都有類似的數據圖表,像制鹽工業手冊,蘭氏化學手冊等一些基礎數據類手冊上都可以查閱到的。